Уважаемые пациенты!
xЛечение рака желудка
Рак желудка — одно из самых распространенных злокачественных новообразований, которое ежегодно уносит жизни свыше 30 тысяч человек в нашей стране и обусловливает практически каждую третью смерть от онкозаболеваний в мире. Каждый год в России диагностируют почти 39 тысяч новых случаев этой патологии, чаще которой встречаются только рак легких и молочной железы. Заболеванию подвержены представители обоих полов, однако мужчины болеют несколько чаще. Пик заболеваемости регистрируется в возрасте свыше 50 лет.
Смертность при раке желудка очень высокая, что является следствием его поздней диагностики. По мнению разных специалистов, у 70-90% пациентов патология выявляется уже на поздних стадиях, когда общий прогноз крайне неблагоприятен, а лечение носит паллиативный и симптоматический характер.
Врачи

Отзывы
28 февраля 2024
Пришлось после операции пройти курс лучевой терапии. Первый раз, когда пришла, конечно боялась. Но эти прекрасные медицинские сотрудники всё доходчиво рассказали. К каждому относяься с пониманием, индивидуально. Очень вежливые, чуткие, доброжелательные. Большое всем спасибо!!! С наступающим всех праздником!!! Всем самого крепкого здоровья, счастья, удачи в вашем нелёгкои труде и самых доброжелательных поциентов!!!❤️❤️❤️

«Здравствуйте, меня зовут Рушана, я живу в городе Казани и оказалась в этом центре, как и многие, наверное, люди нежданно-негаданно для себя. Потому что большую часть своей жизни мы не предполагаем, что мы можем еще с чем-то столкнуться, что в нашей жизни могут быть какие-то серьезные трудности, которые мы еще до этого не преодолевали.
Стоимость лечения
| Наименование услуги | Цена, руб. | Ед. измерения |
|---|---|---|
| Консультация врача онколога радиотерапевта | 1 500 | шт. |
| Повторная консультация специалистов | 500 | шт. |
| Топометрия на специализированном компьютерном томографе первичная | 15 000 | процедура |
| Топометрия на специализированном компьютерном томографе повторная | 7 000 | процедура |
| Дозиметрическое планирование лучевой терапии (томотерапии) первичное | 20 000 | шт. |
| Дозиметрическое планирование лучевой терапии (томотерапии) повторное | 7 000 | шт. |
| Лучевая терапия (томотерапия), включая IMGRT (*) | 314 000 | курс |
| Лучевая терапия (томотерапия) стереотаксическая радиочастотная хирургия (*) | 315 000 | курс |
| Топометрическая разметка | 750 | процедура |
| Проведение исследования плана лучевой терапии по абсолютной дозиметрии на специализированном фантоме “Cheese Phantom Accuray” | 15 000 | процедура |
| Проведение процедуры гарантии качества (QA) плана лучевой терапии на специализированном фантоме “PTW Octavius” | 30 000 | процедура |
Вид лучевой терапии и количество сеансов курса определяется врачебной комиссией индивидуально для каждого пациента исходя из локализации, нозологии опухоли и с учетом анамнеза.
Причины и факторы риска
Сегодня ученым известно, что к формированию рака желудка приводит взаимодействие трех составляющих: Helicobacter pylori, негативное влияние внешних факторов и генетическая предрасположенность.
H.pylori — бактерия, которая колонизирует слизистую желудка и двенадцатиперстной кишки человека. Более чем в 90% случаев это ничем не проявляется, в остальных — приводит к развитию гастритов и язвенной болезни. В 1994 году H.pylori был признан канцерогеном первого порядка. Было установлено, что у носителей бактерии рак желудка развивается в 2-6 раз чаще.
Факторы внешней среды связаны примерно с 80% злокачественных опухолей желудка. Появлению рака способствуют неправильное питание, недостаток антиоксидантов, табакокурение, которое в 2-3 раза увеличивает этот риск. Вместе с тем установлено, что увеличение доли молочных продуктов и фруктов в рационе достоверно сопровождается снижением смертности от рака желудка.
Большинство ученых отмечают связь карцином желудка с фоновыми заболеваниями, которые предшествуют развитию опухоли, но далеко не всегда приводят к ним. К ним относят: состояние после резекции желудка, хронический гиперпластический гастрит, полипы и некоторые патологические процессы.
Клиническая картина
Коварство рака желудка состоит в том, что на ранних стадиях он практически не имеет выраженных симптомов, позволяющих серьезно его заподозрить. Клинически развиваются постепенно с появлением «малых признаков»:
- вялость и апатия;
- повышенная утомляемость;
- нарушения сна и аппетита;
- дискомфорт в области желудка;
- отвращение к мясу.
Эти симптомы настолько неспецифичны, что люди редко придают им значение. Боли в желудке различного характера появляются несколько позже и обычно связываются с погрешностью в диете или иными причинами. Отрыжка, изжога, тошнота и рвота вначале выражены достаточно умеренно, поэтому также не всегда служат причиной обращения к врачу.
По мере роста опухоли нарастает выраженность «малых признаков», к которым присоединяется быстрая потеря массы тела, повышение температуры, анемия. Боли и диспепсические расстройства усиливаются. При этом в целом развитие клинических проявлений зависит от скорости роста новообразования, его локализации, особенностей метастазирования и состояния других органов.
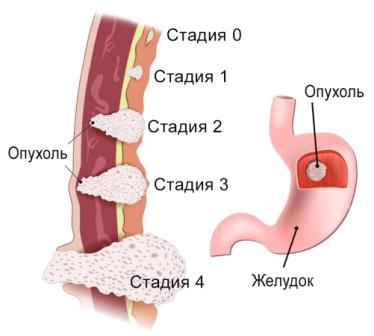
Стадирование рака желудка
Для стадирования используется общепринятая в мире система TNM. При этом новообразования, центр которых располагается менее 5 см от
кардио-эзофагеального перехода и распространяющиеся на пищевод, стадируются по схеме рака пищевода, а остальные — по приведенной ниже классификации.
Т — проникновение первичной опухоли в стенку желудка;
N — вовлечение лимфатических узлов;
М — отдаленные метастазы;
0 — отсутствие признака.
| Стадия | TNM | Описание |
|---|---|---|
| 0 | ТisN0M0 | Тis — рак in situ — патологические изменения в пределах слизистой оболочки до ее собственной пластинки |
| IA | T1N0M0 | Т1 — рост в собственную или мышечную пластинку |
| IB | T2N0M0 T1N1M0 |
Т2 — проникновение в мышечный слой органа; N1 — метастазы в 1-2 лимфоузлах |
| IIA | T3N0M0 T2N1M0 T1N2M0 |
p>T3 — рост в подсерозную клетчатку, а также с инвазией в сальники без проникновения в брюшину;
N2 — до 6 вовлеченных лимфоузлов |
| IIB | T4aN0M0 T3N1M0 T2N2M0 T1N3M0 |
Т4а — инвазия в висцеральный лист брюшины; N3 — 7 и более лимфоузлов |
| IIIA | Т4aN1M0 T3N2M0 T2N3M0 |
|
| IIIB | T4bN0M0 T4bN1M0 T4aN2M0 T3N3M0 |
Т4b — проникновение в соседние органы: кишечник, печень, селезенку, надпочечники. |
| IIIC | T4bN2M0 T4bN3M0 T4aN3M0 |
|
| IV | ТлюбойNлюбойМ1 |
М1 — любые отдаленные метастазы |
На ранних стадиях (I и II) 5-летняя выживаемость достигает 95%. На третьей стадии этот показатель не превышает 20-50%, а на четвертой — 4%. Раннее выявление заболевания помогло бы значительно улучшить прогноз жизни для тысяч людей, однако массовые скрининговые исследования пока остаются для нашей страны экономически недоступными.
Диагностика
Ключевую роль в диагностике играют инструментальные методы исследования, в том числе эндоскопические, лучевые и ультразвуковые.
- Эндоскопическое исследование, и в частности ФГДС — обязательная диагностическая процедура, которая позволяет увидеть и оценить опухоль, а также провести биопсию подозрительных участков на гистологию. Метод отличается высокой специфичностью и чувствительностью (более 90%), и еще более информативен при использовании современных техник визуализации, например, хромоэндоскопии или узкоспектральной визуализации.
- Эндосонография — ультразвуковое исследование, при котором регистрирующий датчик вводится непосредственно в желудок. С его помощью врач может достоверно судить о глубине роста первичной опухоли и ее проникновении в соседние органы, а также наличие вовлеченных лимфоузлов. На ранних этапах опухоли эндоУЗИ позволяет качественно спланировать органосохраняющую операцию.
- Рентгеноконтрастное исследование помогает установить место и протяженность патологического процесса и особенно эффективно при подслизистом росте новообразования, когда результаты биопсии могут быть ложноотрицательными. На ранних стадиях новообразования исследование как правило малоинформативно.
- УЗИ брюшной полости трансабдоминальным датчиком обнаруживает отдаленные метастазы, поражение лимфатических узлов и соседних с желудком структур. На точность исследования оказывает влияние большое число факторов, однако ввиду его простоты, доступности и неинвазивности, оно имеет важное диагностическое значение.
- Компьютерная томография органов грудной клетки и брюшной полости — главный уточняющий метод, позволяющий определить отдаленные метастазы. Являясь более надежным, чем УЗИ, КТ менее доступен, связан с лучевой нагрузкой для пациента и не особо информативен при определении глубины роста.
Помимо перечисленных методов, в зависимости от оснащенности лечебного учреждения и особенностей течения болезни, могут применяться: сонография шейно-надключичных областей, исследование крови на онкомаркеры, анализ биоптата на HER2-neu, колоноскопия, биопсия метастазов под ультразвуковым контролем, ПЭТ-КТ, остеосцинтиграфия и другие процедуры.
Принципы лечения
Основной метод радикального лечения — хирургический, который в некоторых случаях дополняется комбинированными консервативными процедурами. Тактика лечения определяется исходя из особенностей течения заболевания, пациента, технического оснащения, но в целом выглядит следующим образом:
- Ранний рак (стадии 0 и IA ) — органосохраняющие и эндоскопические операции.
- Местнораспространенный рак (стадии IB—III) — радикальное хирургическое или комбинированное лечение.
- Генерализованный рак (стадия V) или рак, при котором операция невозможна ввиду общего состояния организма или иных причин — паллиативное лекарственное лечение.
Эндоскопические операции показаны на ранних стадиях вплоть до стадии IIb в отсутствие метастазов в лимфатические узлы. Рак желудка на ранних стадиях достаточно редко сопровождается метастазированием по лимфатической системе. Например, если рост опухоли ограничен слизистой оболочкой, поражение регионарных лимфоузлов отмечается лишь в 3 % случаев. Это позволят проводить экономные малоинвазивные вмешательства без разрезов передней брюшной стенки.
Хирургическое лечение показано практически всегда за исключением очевидных противопоказаний. Абсолютное противопоказание — отдаленные метастазы, хотя по жизненным показаниям, например при кровотечении, резекция желудка без иссечения лимфоузлов может быть проведена. В зависимости от выраженности опухолевого процесса применяются различные хирургические пособия, основными из которых являются: гастрэктомия (полное удаление желудка) и различные варианты резекции (удаление определенной части органа).
Комбинированное лечение сегодня используется все чаще, поскольку накапливается все больше сведений о преимуществе такого подхода перед чисто хирургическим. Единого мнения в мире по поводу комбинированной терапии сегодня не существует. В азиатском регионе стандартным подходом является адъювантная химиотерапия, начиная со IIа стадии рака желудка, когда пациент получает несколько курсов химиотерапевтических препаратов после операции. В некоторых европейских странах стандартом является периоперационная химиотерапия, которая проводится до и после вмешательства. В США вне зависимости от стадии и локализации опухоли принято проводить послеоперационную химиолучевую терапию. Каждый из этих подходов имеет право на существование, поскольку имеет высокий уровень доказательности.
Применение послеоперационной химиолучевой терапии при раке желудка достаточно ограничено, поскольку, несмотря на несомненную эффективность, такое лечение очень токсично и переносится не всеми пациентами. Огромным шагом вперед стала лучевая терапия под визуальным контролем с модулированной интенсивностью излучения — IG/IMRT, которая позволяет подать необходимую дозу радиации в патологический очаг, минимально затрагивая здоровые ткани. Эта концепция была воплощена в уникальной системе TomoTherapy, которая объединила в себе сканер для компьютерной томографии и высокоточный линейный ускоритель электронов. Основные преимущества TomoTherapy:
- полный радиотерапевтический комплекс в одной установке — контроль, точная укладка и фиксация пациента;
- широкая область применения;
- хорошая переносимость;
- возможность применения в комбинации с другими методоми лечения.
TomoTherapy открывает новые возможности лечения рака желудка, однако такого оборудования в России очень мало — всего два аппарата. Один из них установлен в нашей клинике, где современную медицинскую помощь получают пациенты из разных регионов России.
Часто задаваемые вопросы
Сколько стоит курс лечения?
Курс лечения вместе с предлучевой подготовкой стоит 349 000 рублей. Есть возможность оформления рассрочки на весь период лечения.
Есть ли онлайн-консультация?
Для жителей других регионов, а также для тех, кому визит к врачу затруднителен, наш центр предоставляет возможность бесплатной онлайн - консультации.
Документы, которые необходимы для получения онлайн-консультации?
Для получения консультации о возможности получения томотерапии, вам необходимо направить нам все имеющиеся у вас медицинские выписки и обследования, включая гистологическое заключение. Направление на бесплатную консультацию не требуется.
Возможно ли лечение детей?
Томотерапия наиболее благоприятна для лечения детей, так как лучевая терапия проходит щадящим методом, не задевая здоровые органы и ткани развивающегося ребенка.
На какой стадии можно применять лучевую терапию?
В современной онкологии возможности лучевой терапии применяются очень широко на любой стадии. Однако каждому пациенту требуется индивидуальный подход, так как выбор тактики и плана лечения зависит от многих факторов: расположения опухоли, сопутствующих заболеваний, возраста и общего состояния пациента. Поэтому для получения информации о возможности лечения, необходимо получить консультацию врача-радиотерапевта.
Дата написания: 07.09.18
Дата обновления: 18.08.20
Автор: Аглуллина Мария Викторовна
Проверил: Моров Олег Витальевич
